| | |
 |
 |
 |
Двойная связь
Определение "Двойная связь" в Большой Советской Энциклопедии
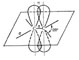
Двойная связь, ковалентная четырёхэлектронная связь между двумя соседними атомами в молекуле. Двойная связь обычно обозначается двумя валентными штрихами: >С=С<, >C=N —, >С=О, >C=S, — N=N —, — Н=О и др. При этом подразумевается, что одна пара электронов с sp2 или sp - гибридизованными орбиталями образует s-связь (см. рис. 1), электронная плотность которой сосредоточена вдоль межатомной оси; s-связь подобна простой связи. Другая пара электронов с р-орбиталями образует p-связь, электронная плотность которой сосредоточена вне межатомной оси. Если в образовании Двойная связь принимают участие атомы IV или V группы периодической системы, то эти атомы и атомы, связанные с ними непосредственно, расположены в одной плоскости; валентные углы равны 120°. В случае несимметричных систем возможны искажения молекулярной структуры. Двойная связь короче простой связи и характеризуется высоким энергетическим барьером внутреннего вращения; поэтому положения заместителей при атомах, связанных Двойная связь, неэквивалентны, и это обусловливает явление геометрической изомерии. Соединения, содержащие Двойная связь, способны к реакциям присоединения. Если Двойная связь электронно-симметрична, то реакции осуществляются как по радикальному (путем гомолиза p-связи), так и по ионному механизмам (вследствие поляризующего действия среды). Если электроотрицательности атомов, связанных Двойная связь, различны или если с ними связаны различные заместители, то p-связь сильно поляризована. Соединения, содержащие полярную Двойная связь, склонны к присоединению по ионному механизму: к электроноакцепторной Двойная связь легко присоединяются нуклеофильные реагенты, а к электронодонорной Двойная связь — электрофильные. Направление смещения электронов при поляризации Двойная связь принято указывать стрелками в формулах, а образующиеся избыточные заряды — символами d- и d+. Это облегчает понимание радикального и ионного механизмов реакций присоединения:

В соединениях с двумя Двойная связь, разделёнными одной простой связью, имеет место сопряжение p-связей и образование единого p-электронного облака, лабильность которого проявляется вдоль всей цепи (рис. 2, слева). Следствием такого сопряжения является способность к реакциям 1,4-присоединения:

Если три Двойная связь сопряжены в шестичленном цикле, то секстет p-электронов становится общим для всего цикла и образуется относительно стабильная ароматическая система (см. рис. 2, справа). Присоединение к подобным соединениям как электрофильных, так и нуклеофильных реагентов энергетически затруднено. (См. также Химическая связь.)
Г. А. Сокольский.
Статья про "Двойная связь" в Большой Советской Энциклопедии была прочитана 873 раз
|
| |
|