


БНБ
"БСЭ" (95279)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Нейтрализация (химич.)
Определение "Нейтрализация (химич.)" в Большой Советской Энциклопедии
Нейтрализация (франц. neutralisation, от лат. neuter — ни тот, ни другой), нейтрализации реакция, химическая реакция между веществом, имеющим свойства кислоты, и веществом, имеющим свойства основания, приводящая к потере характерных свойств обоих соединений (см. Кислоты и основания). При Нейтрализация (химич.) фиксируются свойства кислот, такие, как изменение под их воздействием окраски некоторых растворимых красителей-индикаторов (например, фиолетового лакмуса — в красный цвет), каталитическое действие на некоторые химические реакции (например, инверсия сахаров), растворяющее действие на активные металлы (Mg, Zn и др.), карбонаты и некоторые др. малорастворимые соединения, кислый вкус водных растворов, а также потеря всех этих свойств при реакциях с основаниями. Наиболее типичная реакция нейтрализации в водных растворах происходит между гидратированными ионами водорода (называемыми иначе ионами гидрония) и ионами гидроксила (см. Гидроксильная группа), содержащимися соответственно в сильных кислотах и основаниях:
H3O+ (или Н+×Н2О) + ОН- = 2Н2О.
В результате концентрация каждого из этих ионов становится равной той, которая свойственна самой воде (около 10-7 г = ионов/л при комнатной температуре). При Нейтрализация (химич.) слабой кислоты сильным основанием, например уксусной кислоты едким натром: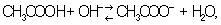
реакция до конца не идёт, является обратимой, и концентрация ионов гидроксила в растворе больше, чем в чистой воде (щелочная реакция раствора). При Нейтрализация (химич.) слабого основания сильной кислотой реакция раствора становится кислой. Следовательно, в обоих последних случаях полная Нейтрализация (химич.) не достигается и водородный показатель (pH) раствора лишь приближается к 7.
В неводных растворах с прототропными растворителями, т. е. такими, которые сами способны принимать или отдавать ионы водорода (протоны), Нейтрализация (химич.) при взаимодействии кислоты и основания наступает тогда, когда концентрация сольватированных ионов водорода в растворе становится равной её концентрации в чистом растворителе. В растворах кислот и оснований непрототропного типа Нейтрализация (химич.) наступает при достижении в реакции нейтрализации той концентрации катионов или анионов, которая свойственна чистому растворителю. Реакции нейтрализации применяются в химических производствах и при обработке отходов в др. производствах, а также в лабораторной практике, особенно в химическом анализе. См. также Нейтрализации методы.
Лит.: Шатенштейн А. И., Теории кислот и оснований, М. — Л., 1949; Дей М. К., Селбин Дж., Теоретическая неорганическая химия, пер, с англ., 2 изд., М., 1971; Денеш И., Титрование в неводных средах, пер. с англ., М., 1971.
Ю. А. Клячко.
| "БСЭ" >> "Н" >> "НЕ" >> "НЕЙ" |
Статья про "Нейтрализация (химич.)" в Большой Советской Энциклопедии была прочитана 963 раз
| Коптим скумбрию в коробке |
| Крабы в кокосовом молоке |
TOP 20
- Лемке Михаил Константинович
- Сульфгидрильные группы
- «Казарменный коммунизм»
- Японское море
- Периодическая система элементов
- Объединённая партия гаитянских коммунистов
- Глициния
- Башкирская Автономная Советская Социалистическая Республика
- Иммунитет (историч.)
- Андаманское море
- Сенсуализм
- Балкано-кавказская раса
- «Сообразительный»
- Навигация (морск.)
- Звёздная астрономия
- Ямполь (пос. гор. типа в Донецкой обл.)
- Кульчицкая Елена Львовна
- Мандельштама - Бриллюэна рассеяние
- Театральные учебные заведения
- Электрическая постоянная