


БНБ
"БСЭ" (95279)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Уравнения химические
Определение "Уравнения химические" в Большой Советской Энциклопедии
Уравнения химические, изображения реакций химических посредством знаков химических, формул химических, чисел и математических знаков. На возможность такого описания химических реакций указал в 1789 А. Лавуазье, основываясь на сохранения массы законе; однако всеобщее применение Уравнения химические получили только в 1-й половине 19 в. Каждое Уравнения химические состоит из двух частей – левой и правой, соединённых знаком равенства (иногда для обозначения направления реакции – простой стрелкой ®, а реакции обратимой – двойной 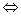 .). В левой части пишут формулы исходных веществ, в правой – формулы полученных веществ; между формулами ставят знак +. При составлении Уравнения химические принимают, что масса полученных веществ равна массе исходных и что число атомов одних и тех же элементов должно быть в обеих частях Уравнения химические одинаковым. Перед формулами исходных и полученных веществ ставят коэффициенты, которые должны быть целыми числами. Например, зная, что при горении метана в кислороде образуются вода и двуокись углерода, можно сразу написать Уравнения химические этой реакции:
.). В левой части пишут формулы исходных веществ, в правой – формулы полученных веществ; между формулами ставят знак +. При составлении Уравнения химические принимают, что масса полученных веществ равна массе исходных и что число атомов одних и тех же элементов должно быть в обеих частях Уравнения химические одинаковым. Перед формулами исходных и полученных веществ ставят коэффициенты, которые должны быть целыми числами. Например, зная, что при горении метана в кислороде образуются вода и двуокись углерода, можно сразу написать Уравнения химические этой реакции:
В более сложных случаях применяют приёмы, описанные в ст. Окисление-восстановление, а также способ, основанный на решении систем неопределённых уравнений. Например, требуется подобрать коэффициент Уравнения химические обжига пирита FeS2 в кислороде:
xFeS2 + yO2 = 2Fe2O3 + tSO2. (2)
Очевидно, что х = 2z, t = 2x, 1y = 3z + 2t. Положив z = 1, имеем: х = 2, t = 4, у = 5,5. Умножив эти числа на 2, получаем: 4FeS2 + 11O2 = 2Fe2O3 + 8SO2.
На основании Уравнения химические делаются расчёты, необходимые в лабораторной и заводской практике.
Лит.: Некрасов Б. В., Основы общей химии, 3 изд., т. 1, М., 1973.
С. А. Погодин.
| "БСЭ" >> "У" >> "УР" >> "УРА" |
Статья про "Уравнения химические" в Большой Советской Энциклопедии была прочитана 1055 раз
| Коптим скумбрию в коробке |
| Коптим скумбрию дома в коробке |
TOP 20
- Лемке Михаил Константинович
- Сульфгидрильные группы
- «Казарменный коммунизм»
- Японское море
- Периодическая система элементов
- Башкирская Автономная Советская Социалистическая Республика
- Объединённая партия гаитянских коммунистов
- Глициния
- Иммунитет (историч.)
- Андаманское море
- Сенсуализм
- Балкано-кавказская раса
- «Сообразительный»
- Звёздная астрономия
- Навигация (морск.)
- Ямполь (пос. гор. типа в Донецкой обл.)
- Мандельштама - Бриллюэна рассеяние
- Театральные учебные заведения
- Кульчицкая Елена Львовна
- Электрическая постоянная