


БНБ
"БСЭ" (95279)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Клапейрона уравнение
Определение "Клапейрона уравнение" в Большой Советской Энциклопедии
Клапейрона уравнение, Клапейрона — Менделеева уравнение, найденная Б. П. Э. Клапейроном (1834) зависимость между физическими величинами, определяющими состояние идеального газа: давлением газа р, его объёмом V и абсолютной температурой Т.
Клапейрона уравнение записывается в виде pV = ВТ, где коэффициент пропорциональности В зависит от массы газа. Д. И. Менделеев, используя Авогадро закон, вывел в 1874 уравнение состояния для 1 моля идеального газа pV = RT, где R — универсальная газовая постоянная. Для газа, имеющего общую массу М и молекулярную массу m,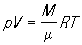 , или pV=NkT,"
, или pV=NkT,"
где N — число частиц газа, k — Больцмана постоянная. Клапейрона уравнение представляет собой уравнение состояния, идеального газа, которое объединяет Бойля — Мариотта закон (зависимость между р и V при Т = const), Гей-Люссака закон (зависимость V от Т при р = const) и Авогадро закон (согласно этому закону, газы при одинаковых значениях р, V и Т содержат одинаковое число молекул N).
Клапейрона уравнение — наиболее простое уравнение состояния, применимое с определённой степенью точности к реальным газам при низких давлениях и высоких температурах (например, атмосферный воздух, продукты сгорания в газовых двигателях и др.), когда они близки по своим свойствам к идеальному газу.
| "БСЭ" >> "К" >> "КЛ" >> "КЛА" >> "КЛАП" |
Статья про "Клапейрона уравнение" в Большой Советской Энциклопедии была прочитана 1121 раз
| Коптим скумбрию в коробке |
| Вкуснейшие куриные леденцы |
TOP 20
- Лемке Михаил Константинович
- Сульфгидрильные группы
- «Казарменный коммунизм»
- Японское море
- Периодическая система элементов
- Объединённая партия гаитянских коммунистов
- Башкирская Автономная Советская Социалистическая Республика
- Глициния
- Иммунитет (историч.)
- Андаманское море
- Сенсуализм
- Балкано-кавказская раса
- «Сообразительный»
- Навигация (морск.)
- Звёздная астрономия
- Ямполь (пос. гор. типа в Донецкой обл.)
- Мандельштама - Бриллюэна рассеяние
- Кульчицкая Елена Львовна
- Театральные учебные заведения
- Электрическая постоянная