


БНБ
"БСЭ" (95279)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Натрий
Определение "Натрий" в Большой Советской Энциклопедии
Натрий (Natrium), Na, химический элемент I группы периодической системы Менделеева; атомный номер 11, атомная масса 22,9898; серебристо-белый мягкий металл, на воздухе быстро окисляющийся с поверхности. Природный элемент состоит из одного стабильного изотопа 23Na.
Историческая справка. Природные соединения Натрий - поваренная соль NaCI, сода Na2CO3 - известны с глубокой древности. Название «натрий», происходящее от араб. натрун, греч. nitron, первоначально относилось к природной соде. Уже в 18 в. химики знали много др. соединений Натрий Однако сам металл был получен лишь в 1807 Г. Дэви электролизом едкого натра NaOH. В Великобритании, США, Франции элемент называется Sodium (от исп. слова soda - сода), в Италии - sodio.
Распространение в природе. Натрий - типичный элемент верхней части земной коры. Среднее содержание его в литосфере 2,5% по массе, в кислых изверженных породах (граниты и др.) 2,77, в основных (базальты и др.) 1,94, в ультраосновных (породы мантии) 0,57. Благодаря изоморфизму Na+ и Ca2+, обусловленному близостью их ионных радиусов, в магматических породах образуются натриево- href="http://Ca-Calcium.info/">кальциевые полевые шпаты (плагиоклазы). В биосфере происходит резкая дифференциация Натрий: осадочные породы в среднем обеднены Натрий (в глинах и сланцах 0,66%), мало его в большинстве почв (среднее 0,63%). Общее число минералов Натрий 222. Na слабо задерживается на континентах и приносится реками в моря и океаны, где его среднее содержание 1,035% (Na - главный металлический элемент морской воды). При испарении в прибрежно-морских лагунах, а также в континентальных озёрах степей и пустынь осаждаются соли Натрий, формирующие толщи соленосных пород. Главные минералы, являющиеся источником Натрий и его соединений, - галит (каменная соль) NaCI, чилийская селитра NaNO3, тенардит Na2SO4, мирабилит Na2SO4·10H2O, трона NaH (CO3)2×2H2O. Мировая добыча Натрий оценивается 1×108 т. Na - важный биоэлемент, в живом веществе в среднем содержится 0,02% Na; в животных его больше, чем в растениях.
Физические и химические свойства. При обычной температуре Натрий кристаллизуется в кубической решётке, а = 4,28 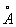 . Атомный радиус 1,86
. Атомный радиус 1,86 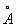 , ионный радиус Na+ 0,92
, ионный радиус Na+ 0,92 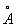 . Плотность 0,968 г/см3 (19,7 °С), tпл 97,83 °С, tkип 882,9 °С; удельная теплоёмкость (20 °С) 1,23×103 дж/(кг×К) или 0,295 кал/(г×град); коэффициент теплопроводности 1,32×102 вт/(м×К) или 0,317 кал/(см×сек×град); температурный коэффициент линейного расширения (20 °С) 7,1×10-5 удельное электрическое сопротивление (0 °С) 4,3·0-8 ом×м (4,3·0-6 ом×см). Натрий парамагнитен, удельная магнитная восприимчивость + 9,2×10-6; весьма пластичен и мягок (легко режется ножом).
. Плотность 0,968 г/см3 (19,7 °С), tпл 97,83 °С, tkип 882,9 °С; удельная теплоёмкость (20 °С) 1,23×103 дж/(кг×К) или 0,295 кал/(г×град); коэффициент теплопроводности 1,32×102 вт/(м×К) или 0,317 кал/(см×сек×град); температурный коэффициент линейного расширения (20 °С) 7,1×10-5 удельное электрическое сопротивление (0 °С) 4,3·0-8 ом×м (4,3·0-6 ом×см). Натрий парамагнитен, удельная магнитная восприимчивость + 9,2×10-6; весьма пластичен и мягок (легко режется ножом).
Нормальный электродный потенциал Натрий 2,74 в; электродный потенциал в расплаве - 2,4 в. Пары Натрий окрашивают пламя в характерный ярко-жёлтый цвет. Конфигурация внешних электронов атома 3s1; во всех известных соединениях Натрий одновалентен. Его химическая активность очень высока. При непосредственном взаимодействии с кислородом в зависимости от условий образуются окись Na2O или перекись Na2O2 - бесцветные кристаллические вещества. С водой Натрий образует гидроокись NaOH и Н2; реакция может сопровождаться взрывом. Минеральные кислоты образуют с Натрий соответствующие растворимые в воде соли, однако по отношению к 98-100%-ной серной кислоте Натрий сравнительно инертен.
Реакция Натрий с водородом начинается при 200 °С и приводит к получению гидрида NaH - бесцветного гигроскопичного кристаллического вещества. С фтором и хлором Натрий взаимодействует непосредственно уже при обычной температуре, с бромом - только при нагревании; с йодом прямого взаимодействия не наблюдается. С серой реагирует бурно, образуя натрия сульфид. Взаимодействие паров Натрий с азотом в поле тихого электрического разряда приводит к образованию нитрида Na3N, а с углеродом при 800-900 °С - к получению карбида Na2C2.
Натрий растворяется в жидком аммиаке (34,6 г на 100 г NH3 при 0 °С) с образованием аммиачных комплексов. При пропускании газообразного аммиака через расплавленный Натрий при 300-350 °С образуется натрийамин NaNH2 - бесцветное кристаллическое вещество, легко разлагаемое водой. Известно большое число натрийорганических соединений, которые по химическим свойствам весьма сходны с литийорганическими соединениями, но превосходят их по реакционной способности. Применяют натрийорганические соединения в органическом синтезе как алкилирующие агенты.
Натрий входит в состав многих практически важных сплавов. Сплавы Na - К, содержащие 40-90% К (по массе) при температуре около 25 °С, - серебристо-белые жидкости, отличающиеся высокой химической активностью, воспламеняющиеся на воздухе. Электропроводность и теплопроводность жидких сплавов Na - К ниже соответствующих величин для Na и К. Амальгамы Натрий легко получаются при введении металлического Натрий в ртуть; при содержании свыше 2,5% Na (по массе) при обычной температуре являются уже твёрдыми веществами.
Получение и применение. Основной промышленный метод получения Натрий - электролиз расплава поваренной соли NaCI, содержащей добавки KCI, NaF, CaCl2 и др., которые снижают температуру плавления соли до 575-585 °С. Электролиз чистого NaCI привёл бы к большим потерям Натрий от испарения, т.к. температуры плавления NaCI (801 °С) и кипения Na (882,9 °С) очень близки. Электролиз проводят в электролизёрах с диафрагмой, катоды изготовляют из железа или меди, аноды - из графита. Одновременно с Натрий получают хлор. Сохранился и старый способ получения Натрий - электролиз расплавленного едкого натра NaOH, который значительно дороже NaCI, однако электролитически разлагается при более низкой температуре (320-330 °С).
Натрий и его сплавы широко применяются как теплоносители для процессов, требующих равномерного обогрева в интервале 450-650 °С - в клапанах авиационных двигателей и особенно в ядерных энергетических установках. В последнем случае жидко-металлическими теплоносителями служат сплавы Na - К (оба элемента имеют малые сечения поглощения тепловых нейтронов, для Na 0,49 барн); эти сплавы отличаются высокими температурами кипения и коэффициентами теплопередачи и не взаимодействуют с конструкционными материалами при высоких температурах, развиваемых в энергетических ядерных реакторах. Соединение NaPb (10% Na по массе) применяется в производстве тетраэтилсвинца-наиболее эффективного антидетонатора. В сплаве на основе свинца (0,73% Ca, 0,58% Na и 0,04% Li), применяемом для изготовления осевых подшипников ж.-д. вагонов, Натрий является упрочняющей добавкой. В металлургии Натрий служит активным восстановителем при получении некоторых редких металлов (Ti, Zr, Ta) методами металлотермии; в органическом синтезе - в реакциях восстановления, конденсации, полимеризации и др. О применении соединений Натрий см. Натрия бромид, Натрия гидроокись, Натрия сульфат, Натрия хлорид, Натриевая селитра, Сода и др.
Вследствие большой химической активности Натрий обращение с ним требует осторожности. Особенно опасно попадание на Натрий воды, которое может привести к пожару и взрыву. Глаза должны быть защищены очками, руки - толстыми резиновыми перчатками; соприкосновение Натрий с влажной кожей или одеждой может вызвать тяжёлые ожоги.
В. Е. Плющев.
Натрий в организме. Натрий - один из основных элементов, участвующих в минеральном обмене животных и человека. Содержится главным образом во внеклеточных жидкостях (в эритроцитах человека около 10 ммоль/кг, в сыворотке крови 143 ммоль/кг); участвует в поддержании осмотического давления и кислотно-щелочного равновесия, в проведении нервных импульсов (см. Мембранная теория возбуждения). Суточная потребность человека в хлористом натрии колеблется от 2 до 10г и зависит от количества этой соли, теряемой с потом. Концентрация ионов Натрий в организме регулируется в основном гормоном коры надпочечников - альдостероном. Несмотря на относительно высокое содержание Натрий в тканях растений (около 0,01% на сырую массу), его роль в жизни растений изучена недостаточно. У галофитов (виды, произрастающие на сильно засоленных почвах) Натрий создаёт высокое осмотическое давление в клеточном соке и тем самым способствует извлечению воды из почвы. См. также Водно-солевой обмен.
И. Ф. Грибовская.
В медицине из препаратов Натрий наиболее часто применяют натрия сульфат, хлорид NaCI (при кровопотерях, потерях жидкости, рвоте и т.п.), борат Na2B4O7×10H2O (как антисептическое средство), гидрокарбонат NaHCO3 (как отхаркивающее средство, а также для промываний и полосканий при ринитах, ларингитах и др.), тиосульфат Na2S2O3×5H2O (противовоспалительное, десенсибилизирующее и противотоксическое средство) и цитрат Na3C6H5O7×51/2H2O (препарат из группы антикоагулянтов).
Искусственно полученные радиоактивные изотопы 22Na (период полураспада T1/2 = 2,64 г.) и 24Na (T1/2 = 15 ч) применяют для определения скорости кровотока в отдельных участках кровеносной системы при сердечно-сосудистых и лёгочных заболеваниях, облитерирующем эндартериите и др. Радиоактивные растворы солей Натрий (например, 24NaCI) используют также для определения сосудистой проницаемости, изучения общего содержания обменного Натрий в организме, водно-солевого обмена, всасывания из кишечника, процессов нервной деятельности и в некоторых др. экспериментальных исследованиях.
М. Д. Дорфман.
Лит.: Ситтиг М., Натрий, его производство, свойства и применение, пер. с англ., М., 1961; Ullmanns Encykiopädie der technihen Chemie, 3 Aufl., Bd 12, Münch. - B., 1960: Реформатский И. А., Натрий, в кн.: Краткая химическая энциклопедия, т. 3, М., 1964; Рипан Р., Четяну И., Неорганическая химия, т. 1, пер. с рум., М., 1971; Проссер Л., Браун Ф., Сравнительная физиология животных, пер. с англ., М., 1967.
| "БСЭ" >> "Н" >> "НА" >> "НАТ" |
Статья про "Натрий" в Большой Советской Энциклопедии была прочитана 592 раз
| Вкуснейшие куриные леденцы |
| Вкуснейшие куриные леденцы |
TOP 20
- Лемке Михаил Константинович
- Сульфгидрильные группы
- «Казарменный коммунизм»
- Глициния
- Японское море
- Периодическая система элементов
- Башкирская Автономная Советская Социалистическая Республика
- Иммунитет (историч.)
- Андаманское море
- Сенсуализм
- «Сообразительный»
- Звёздная астрономия
- Балкано-кавказская раса
- Ямполь (пос. гор. типа в Донецкой обл.)
- Навигация (морск.)
- Кульчицкая Елена Львовна
- Мандельштама - Бриллюэна рассеяние
- Театральные учебные заведения
- Электрическая постоянная
- Энсор Джеймс