


БНБ
"БСЭ" (95279)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Атом
Определение "Атом" в Большой Советской Энциклопедии
 |
| Возможные состояния атома водорода |
 |
| Заполнения уровней энергии отдельного электрона в сложном атоме |
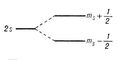 |
| Расщепление уровня энергии во внешнем магнитном поле |
 |
| Энергия атома водорода |
Характерные порядки размеров:
| Линейные размеры | Площадь* | Объем |
| Атом | 10—8 см | 10—16 см2 | 10—24 см3 |
| Ядро | 10—12 см | 10—24 см2 | 10—36 см3 |
| Отношение | 104 | 108 | 1012 |
* Поперечное сечение.
Электронные оболочки Атом не имеют строго определённой границы; значения размеров Атом в большей или меньшей степени зависят от способов их определения и весьма разнообразны (см. Атомные радиусы).
Заряд ядра — основная характеристика Атом, обусловливающая его принадлежность определённому элементу. Заряд ядра всегда является целым кратным элементарного положительного электрич. заряда е, равного по абсолютному значению заряду электрона —е. Заряд ядра равен +Ze, где Z — порядковый номер (атомный номер). Z = 1, 2, 3, 4,... для Атом последовательных элементов в периодической системе элементов Менделеева, т. е. для атомов Н, Не, Li, Be, ...В нейтральном Атом ядро с зарядом +Ze удерживает Z электронов с общим зарядом —Ze и полный заряд Атом равен нулю; в положительном ионе —Атом, потерявшем k электронов (ионизованном Атом), остаётся Z—k электронов (k = 1, 2, 3, ... — кратность ионизации) и его заряд равен +ke, в отрицательном ионе —Атом, присоединившем k электронов,— содержится Z + k электронов, и его заряд равен —ke. Для положительного иона максимальное значение k = Z (такой ион потерял все свои электроны и состоит из «голого» ядра); для отрицательного свободного иона k = 1, для связанных Атом возможно образование отрицательных ионов с k > 1 (в растворах, комплексных соединениях и ионных кристаллах). Говоря об Атом определённого элемента, подразумевают как нейтральные Атом, так и ионы этого элемента. Но иногда под Атом понимают нейтральный Атом, в противоположность ионам. Положительные и отрицательные ионы при написании отличают от нейтрального Атом индексом k+ и k—, например О обозначает нейтральный Атом кислорода (Z = 8), О+, О2+(или O++), O3+,..., O8+ — его положительные ионы,О—, O2— (или О— — его отрицательные ионы. Совокупность нейтрального Атом и ионов других элементов с тем же числом электронов образует изоэлектронный ряд. Простейший такой ряд начинается с Атом водорода: H, He+, Li2+, Be3+, ...; члены этого ряда состоят из ядра и одного электрона.
Порядок значений зарядов ядер различных Атом был определён английским физиком Э. Резерфордом в его первоначальных опытах по рассеянию альфа-частиц (1911). Значения Z были надёжно установлены английским физиком Г. Мозли (1913—14) на основе изучения рентгеновских спектров последовательных элементов в периодической системе. Кратность заряда ядра Атом элементарному заряду е получила объяснение, исходя из представлений о строении ядра: Z равно числу протонов в ядре, протон имеет заряд +е, и полный заряд ядра равен сумме зарядов всех Z протонов, т. е. +Ze.
Масса атома возрастает с увеличением Z. Масса ядра Атом приближённо пропорциональна массовому числу А — общему числу протонов и нейтронов в ядре. Масса электрона (0,91 10—27 г) значительно меньше (примерно в 1840 раз) массы протона или нейтрона (1,67 10—24 г), и поэтому масса Атом в целом определяется в основном массой его ядра.
Атом данного элемента могут отличаться массой ядра (число протонов Z постоянно, число нейтронов А—Z может меняться); такие разновидности Атом одного и того же элемента называются изотопами. Различие массы ядра почти не сказывается на строении их электронных оболочек, зависящем от заряда ядра Z. Химические и большинство физических свойств (оптические, электрические, магнитные), определяемые строением электронных оболочек, одинаковы или очень близки для всех изотопов данною элемента. Наибольшие отличия в свойствах (изотонические эффекты) получаются для изотопов водорода (Z = 1) из-за большой разницы в массах обычного лёгкого Атом водорода (А = 1), Атом дейтерия (А = 2) и Атом трития (А = 3).
Масса Атом приближённо равна массовому числу А и изменяется от 1,67 10—24 г для самого лёгкого Атом водорода (основного изотопа: Z = 1, A = 1) до примерно 4 10—22 г для самых тяжёлых Атом трансурановых элементов (Z = 100, А = 250).
Наиболее точные значения масс Атом могут быть определены методами масс-спектроскопии. Масса Атом не равна в точности сумме массы ядра и масс электронов, а несколько меньше — на дефект массы DМ = W/c2", где W — энергия образования Атом из ядра и электронов, а с — скорость света. Эта поправка — порядка массы одного электрона mе для тяжёлых Атом, а для лёгких Атом пренебрежимо мала (порядка 10—4 массы электрона).
Энергия атома и её квантование. Благодаря малым размерам и большой массе ядра его можно приближённо считать точечным и покоящимся в центре масс Атом (общий центр масс ядра и электронов находится вблизи ядра, а скорость движения ядра относительно центра масс Атом мала по сравнению со скоростями движения электронов). Соответственно Атом можно рассматривать как систему, в которой N электронов с зарядами —е движутся вокруг неподвижного притягивающего центра. Движение электронов в Атом происходит в ограниченном объёме — оно является связанным. Полная внутренняя энергия Атом Е равна сумме кинетических энергий всех электронов Т и потенциальной энергии U — энергии притяжения их ядром и отталкивания их друг от друга (электростатической энергии взаимодействия электрических зарядов ядра и электронов, согласно закону Кулона).
В простейшем случае Атом водорода один электрон с зарядом —е движется вокруг неподвижного центра с зарядом +е. В этом случае, согласно классической механике, кинетическая энергия
Т =1/2mv =p2/2m (1)
где m — масса, v — скорость, p = mv — количество движения (импульс) электрона. Потенциальная энергия (сводящаяся к энергии притяжения электрона ядром)
U = U(r) = —e2/r (2)
и зависит только от расстояния r электрона от ядра. Графически функция U(r) изображается кривой (рис. 1, а), неограниченно убывающей при уменьшении r, т. е. при приближении электрона к ядру. Значение U (r) на бесконечности принято за нуль. При отрицательных значениях полной энергии Е = Т + U < 0 движение электрона является связанным: оно ограничено в пространстве значениями r = rmax, при которых Т = 0, Е = U(rmax). При положительных значениях полной энергии E = T + U > 0 движение электрона является свободным — он может уйти на бесконечность с энергией Е = Т = 1/2 mv2, что соответствует ионизованному Атом водорода Н+. Нейтральный Атом водорода Н представляет, т. о., систему, состоящую из ядра и электрона в связанном состоянии с энергией E < 0.
Полная внутренняя энергия Атом Е является его основной характеристикой как квантовой системы — системы, подчиняющейся квантовым законам (см. Квантовая механика). Как показывает огромный экспериментальный материал (см., например, Франка—Герца опыт), Атом может длительно находиться лишь в состояниях с определённой энергией — стационарных (неизменных во времени) состояниях.
Существование стационарных состояний — один из основных законов физики микроскопических явлений — квантовой физики. Внутренняя энергия квантовой системы, состоящей из связанных микрочастиц (такой системой и является Атом), может принимать одно из дискретного (прерывного) ряда значений
E1, E2, E3, ...(E1 < E2 < E3 < ...). (3)
Каждому из этих «дозволенных» значений энергии соответствует одно или несколько стационарных квантовых состояний движения. Промежуточными значениями энергии (например, лежащими между E1 и E2, E2 и E3 и т.д.) система обладать не может, о такой системе говорят, что её энергия квантована, а нахождение возможных значений энергии называется квантованием энергии. Любое изменение энергии Е связано с квантовым (скачкообразным) переходом системы из одного стационарного квантового состояния в другое (см. ниже).
Графически возможные дискретные значения энергии (3) Атом можно изобразить, по аналогии с потенциальной энергией тела, поднятого на различные высоты (на различные уровни), в виде схемы уровней энергии, где каждому значению энергии соответствует прямая, проведённая на высоте Ei (i = 1, 2, 3, ...); такая схема приведена на рис. 1, б для Атом водорода (на рис. 1, а при E < 0 оказываются, т. о., возможными лишь определённые ступеньки, соединённые горизонтальным пунктиром с уровнями схемы на рис. 1, б). Самый нижний уровень Ei, соответствующий наименьшей возможной энергии системы, называется основным, а все остальные (Ei > Ei, г = 2, 3, 4, ...) — возбуждёнными, т. к. для перехода на них (перехода в соответствующие стационарные возбуждённые состояния из стационарного основного состояния) необходимо возбудить систему — сообщить ей извне энергию Ei—E1.
Квантование энергии Атом является следствием волновых свойств электронов. Нельзя считать, что электрон в Атом движется как материальная точка по определённой траектории, согласно законам классической механики. Эти законы справедливы лишь для частиц большой массы (макрочастиц), а для электрона, как микрочастицы, необходимо учитывать, наряду с его корпускулярными свойствами (свойствами частицы), и его волновые свойства. Согласно квантовой механике, движению микрочастицы массы m со скоростью v соответствует длина волны l = h/mv, где h — Планка постоянная. Для электрона в Атом l ~ 10—8 см, т. е. порядка линейных размеров Атом, и учёт волновых свойств электрона в Атом является необходимым. Связанное движение электрона в Атом схоже со стоячей волной, и его следует рассматривать не как движение материальной точки по траектории, а как сложный колебательный процесс. Для стоячей волны в ограниченном объёме возможны лишь определённые значения длины волны l (и, следовательно, частоты колебаний v). Так как, согласно квантовой механике, v = E/h, отсюда следует, что система, состоящая, подобно Атом, из связанных микрочастиц, может иметь лишь определённые значения энергии, т. е. энергия квантуется и получается дискретная последовательность уровней энергии — дискретный энергетический спектр. Для Атом водорода такая дискретная последовательность получается при Е < 0 (см. рис. 1). Свободное, т. е. не ограниченное в пространстве, поступательное движение микрочастицы, например движение электрона, оторванного от Атом (в случае Атом водорода — электрона с энергией Е > 0), сходно с распространением бегущей волны в неограниченном объёме, для которой возможны любые значения l (и v). Энергия такой свободной микрочастицы может принимать любые значения, т. е. не квантуется, и получается непрерывная последовательность уровней энергии — непрерывный энергетический спектр. Для Атом водорода такая непрерывная последовательность, соответствующая ионизованному Атом, получается при E > 0. Значение Е ¥ = 0 соответствует границе ионизации, а разность Е ¥ — Е1 = Еион представляет энергию ионизации: для Атом водорода она равна 13,6 эв.
Распределение электронной плотности. Состояние электрона в Атом можно характеризовать распределением в пространстве его электрического заряда с некоторой плотностью — распределением электронной плотности. При этом электроны рассматриваются наглядным образом, как «размазанные» в пространстве и образующие «электронное облако». Такая модель правильнее характеризует электроны в Атом, чем модель точечного электрона, движущегося, согласно теории Бора (см. Атомная физика), по строго определённым орбитам. Вместе с тем боровским орбитам можно сопоставить определённые распределения электронной плотности. Для основного уровня энергии Е1 электронная плотность концентрируется вблизи ядра; для возбуждённых уровней энергии E2, E3, E4,... она распределяется на всё больших средних расстояниях от ядра (что соответствует возрастанию размера орбит в теории Бора). В сложном Атом эти электроны группируются в оболочки, окружающие ядро на различных расстояниях и характеризующиеся определёнными распределениями электронной плотности. Прочность связи электронов в более внешних оболочках меньше, чем во внутренних, и слабее всего электроны связаны в самой внешней оболочке, обладающей наибольшими размерами, которые и определяют размеры Атом в целом. При ионизации Атом теряет внешние электроны; размеры положительных ионов тем меньше размеров нейтрального Атом, чем выше кратность иона. Наоборот, размеры отрицательных ионов больше размеров нейтрального Атом
Учёт спина электрона и спина ядра. В теории Атом весьма существен учёт спина электрона — его собственного (спинового) момента количества движения, с наглядной точки зрения соответствующего вращению электрона вокруг собственной оси (если электрон рассматривать как частицу малых размеров). Со спином электрона связан его магнитный момент. Поэтому в Атом необходимо учитывать, наряду с электростатическими взаимодействиями (см. выше), и магнитные взаимодействия, определяемые спиновым магнитным моментом, а также орбитальным магнитным моментом, связанным с движением электрона вокруг ядра; магнитные взаимодействия малы по сравнению с электростатическими. Наиболее существенное влияние спина проявляется в сложных Атом: от спина электронов зависит заполнение электронных оболочек Атом определённым числом электронов (см. ниже).
Ядро в Атом также может обладать собственным механическим моментом — ядерным спином, с которым связан небольшой ядерный магнитный момент (в сотни и тысячи раз меньший электронного магнитного момента), а в некоторых случаях и т. н. квадрупольный электрический момент (см. Моменты атомных ядер). Это приводит к дополнительным очень малым взаимодействиям ядра и электронов, обусловливающим дополнительное расщепление уровней энергии Атом — т. н. сверхтонкую структуру (малую по сравнению с тонкой структурой).
Квантовые состояния атома водорода. Важнейшую роль в квантовой теории Атом играет теория простейшего одноэлектронного Атом, состоящего из ядра с зарядом +Ze и электрона с зарядом —е, — теория Атом водорода Н и водородоподобных ионов Не+, Li2+, Ве3+,... (изоэлектронного ряда, см. выше), называется обычно теорией Атом водорода. Методами квантовой механики можно получить точную и полную характеристику состояний электрона в одноэлектронном Атом Задача о сложных (многоэлектронных) атомах решается лишь приближённо; при этом исходят из результатов решения задачи об одноэлектронном Атом
Уровни энергии Атом водорода и водородоподобных ионов. Энергия одноэлектронного Атом (без учёта спина электрона) равна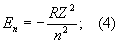
целое число n = 1, 2, 3, ... определяет возможные дискретные значения энергии — уровни энергии; его называют главным квантовым числом. R — Ридберга постоянная, равная 13,6 эв. Уровни энергии Атом водорода на схеме рис. 1, б построены для Z = 1 согласно формуле (4); они сгущаются (сходятся) к границе ионизации Е¥ = 0, соответствующей n = ¥ (уровни энергии с n > 5 на схеме не показаны). Для водородоподобных ионов изменяется (в Z2 раз) лишь масштаб энергий. Энергия ионизации водородоподобного Атом (энергия связи электрона в таком Атом) равна (в эв)
Еион = E¥ — E1 = RZ2 = 13,6Z2 (5)
что даёт для Н, Не+, Li2+, ... значения 13,6 эв, 54,4 эв, 122,4 эв, ...
Основная формула (4) соответствует выражению U (r) = —Ze2/r для потенциальной энергии электрона, притягиваемого ядром с зарядом +Ze [см. (2) и рис. 1, а для случая Z = 1]. Эта формула была впервые выведена Н. Бором в его теории Атом (1913) путём рассмотрения движения электрона вокруг ядра по круговой орбите радиуса r. Уровням энергии (4) соответствуют орбиты радиуса
anZ = a0n2/Z (6)
где постоянная a0 = 0,529 10—8см = 0,529 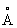 — радиус первой круговой орбиты Атом водорода, соответствующей его основному уровню (этим боровским радиусом часто пользуются в качестве удобной единицы для измерений длин в атомной физике). Радиус орбит пропорционален квадрату главного квантового числа n2 и обратно пропорционален Z; для водородоподобных ионов масштаб линейных размеров уменьшается в Z раз по сравнению с Атом водорода.
— радиус первой круговой орбиты Атом водорода, соответствующей его основному уровню (этим боровским радиусом часто пользуются в качестве удобной единицы для измерений длин в атомной физике). Радиус орбит пропорционален квадрату главного квантового числа n2 и обратно пропорционален Z; для водородоподобных ионов масштаб линейных размеров уменьшается в Z раз по сравнению с Атом водорода.
Характеристика квантовых состояний атома водорода. Согласно квантовой механике, состояние Атом водорода полностью определяется дискретными значениями четырёх физических величин: энергии Е, орбитального момента Ml, (момента количества движения электрона относительно ядра); проекции Mlz орбитального момента на направление z (выбранное произвольно в пространстве); проекции Msz спинового момента (собственного момента количества движения электрона Ms). Возможные значения этих физических величин, в свою очередь, определяются соответствующими квантовыми числами:
1) Е — по закону (4) — главным квантовым числом n =1, 2, 3, ...;
2) Мl — по закону Ml2 = (h2/4p2)l(l + 1) [при l " 1, Ml2 = (h2/4p2)l2 — орбитальным (или азимутальным) квантовым числом l = 0,1, 2, ..., n—1;
3) Mlz — по закону Mlz = (h/2p)mlz — магнитным орбитальным квантовым числом ml = l, l—1, ..., —l;
4) Msz — по закону Msz = (h/2p)ms — магнитным спиновым квантовым числом ms = 1/2, —1/2.
Значения квантовых чисел n, l, ml, ms и характеризуют состояние электрона в Атом водорода. Энергия Атом водорода зависит только от n, и уровню энергии с заданным n соответствует ряд состояний, отличающихся значениями l, ml и ms. Состояния с заданными значениями n и l принято обозначать как 1s, 2s, 2p, 3s, ..., где цифры указывают значение n, а буквы s, р, d, f (дальше по латинскому алфавиту) — соответственно значения l = 0, 1, 2, 3, ... При заданных n и l число различных состояний равно 2(2l + 1) — числу комбинаций значений ml и ms (первое принимает 2l + 1 значение, второе — 2 значения). Общее число различных состояний с заданными n и l при учёте, что l может принимать значения от 0 до n—1, получается равным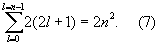
Т. о., каждому уровню энергии Атом водорода соответствует 2, 8, 18, ..., 2n2 (при n = 1, 2, 3, ...) различных стационарных квантовых состояний (рис. 2). Если уровню энергии соответствует лишь одно квантовое состояние, то его называют невырожденным, если два или более — вырожденным (см. Вырождение), а число таких состояний g называются степенью или кратностью вырождения (для невырожденных уровней энергии g = 1). Уровни энергии Атом водорода являются вырожденными, а их степень вырождения gn = 2n2.
Для различных состояний Атом водорода получается и различное распределение электронной плотности. Оно зависит от квантовых чисел n, l и /mi/. При этом электронная плотность для s-cocтояний (l = 0) отлична от нуля в центре, т. е. в месте нахождения ядра, и не зависит от направления (сферически симметрична), а для остальных состояний (l > 0) она равна нулю в центре и зависит от направления. Распределение электронной плотности для состояний Атом водорода с n = 1, 2 и 3 показано на рис. 3 (оно получено фотографированием специальных моделей); размеры «электронного облака» растут примерно пропорционально n2(масштаб на рис. 3 уменьшается при переходе от n = 1 к n = 2 и от n = 2 к n = 3), что соответствует увеличению радиуса орбит по формуле (6) в теории Бора.
Квантовые состояния электрона в водородоподобных ионах характеризуются теми же четырьмя квантовыми числами n, l, ml и ms, что и в Атом водорода. Сохраняется и распределение электронной плотности, только она увеличивается в Z раз и на рис. 3 масштабы нужно уменьшить также в Z раз. Соответственно уменьшаются и размеры орбит.
Действие внешних полей на уровни энергии атома водорода. Во внешнем электрическом и магнитном полях Атом как электрическая система приобретает дополнительную энергию. Электрическое поле поляризует Атом — смещает электронное облако относительно ядра, а магнитное поле ориентирует определённым образом магнитный момент Атом, связанный с движением электрона вокруг ядра (с орбитальным моментом Ml) и его спином. Различным состояниям Атом водорода с той же энергией Еn во внешнем поле соответствует различная дополнительная энергия DE и вырожденный уровень энергии Еn расщепляется на ряд подуровней (рис. 4). Как расщепление в электрическом поле — Штарка явление, так и расщепление в магнитном поле — Зеемана явление, для уровней энергии Атом водорода пропорциональны напряжённости полей.
К расщеплению уровней энергии приводят и малые магнитные взаимодействия внутри Атом Для Атом водорода и водородоподобных ионов имеет место спин-орбитальное взаимодействие — взаимодействие спинового и орбитального моментов электрона, не учитываемое при выводе основной формулы (4); оно обусловливает т.н. тонкую структуру уровней энергии — расщепление возбуждённых уровней Еn (при n > 1) на подуровни. Наиболее точные исследования тонкой структуры методами радиоспектроскопии показали наличие т. н. сдвига уровней, объясняемого в квантовой электродинамике.
Для всех уровней энергии Атом водорода наблюдается и сверхтонкая структура, обусловленная очень малыми магнитными взаимодействиями ядерного спина с электронными моментами. Уровень E1 расщепляется на 2 подуровня с расстоянием между ними примерно 5 10—6 эв.
Электронные оболочки сложных атомов. Теория сложных Атом, содержащих 2 или более электронов, принципиально отличается от теории Атом водорода, т. к. в сложном Атом имеются взаимодействующие друг с другом одинаковые частицы — электроны. Взаимное отталкивание электронов в многоэлектронном Атом существенно уменьшает прочность их связи с ядром. Например, энергия отрыва единственного электрона в ионе гелия (Не+) равна 54,4 эв, в нейтральном же атоме гелия в результате отталкивания электронов энергия отрыва одного из них уменьшается до 24,6 эв. Для внешних электронов более тяжёлых Атом уменьшение прочности их связи из-за отталкивания внутренними электронами ещё более значительно. Чрезвычайно важную роль в сложных Атом играют свойства электронов как одинаковых микрочастиц (см. Тождественности принцип), обладающих спином s = 1/2, для которых справедлив Паули принцип. Согласно этому принципу, в системе электронов не может быть более одного электрона в каждом квантовом состоянии, что для сложного Атом приводит к образованию электронных оболочек, заполняющихся строго определёнными числами электронов.
Учитывая неразличимость взаимодействующих между собой электронов, имеет смысл говорить только о квантовых состояниях Атом в целом. Однако приближённо можно рассматривать квантовые состояния отдельных электронов и характеризовать каждый из них совокупностью четырёх квантовых чисел n, l, ml и ms, аналогично электрону в Атом водорода. При этом энергия электрона оказывается зависящей не только от n, как в Атом водорода, но и от l; от ml; и ms она по-прежнему не зависит. Электроны с данными n и l в сложном Атом имеют одинаковую энергию и образуют определённую электронную оболочку; их называют эквивалентными электронами. Такие электроны и образованные ими оболочки обозначают, как и квантовые состояния и уровни энергии с заданными n и l, символами ns, nр, nd, nf, ... (для l = 0, 1, 2, 3 ....) и говорят о 2р-электронах, 3s-oболочках и т. п.
Заполнение электронных оболочек и слоёв. В силу принципа Паули любые 2 электрона в Атом должны находиться в различных квантовых состояниях и, следовательно, отличаться хотя бы одним из четырёх квантовых чисел n, l, ml и ms. Для эквивалентных электронов (n и l одинаковы) должны быть различны пары значений mi и ms. Число таких пар равно числу различных квантовых состояний электрона с заданными n иl, т. е. степени вырождения его уровня энергии. Это число gl = 2 (2l + 1) = 2, 6, 10, 14, ... и определяет число электронов, полностью заполняющих данную оболочку. Т. о., s-, р-, d-, f-, ... оболочки заполняются 2, 6, 10, 14, ... электронами, независимо от значения n. Электроны с данным n образуют слой, состоящий из оболочек с l = 0, 1, 2, ..., n—1 и заполняемый 2n2 электронами, т. н. К-, L-, М-, N-, ...слой. При полном заполнении имеем:
| n | 1 | 2 | 3 | 4 |
| Слои | К-слой | L-слой | M-слой | N-слой |
| l | 0 | 0 1 | 0 1 2 | 0 1 2 3 |
| Оболочки | 1s | 2s 2p | 3s 3p 3d | 4s 4p 4d 4f |
| Число электронов в слое | 2 | 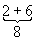 | 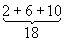 | 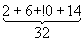 |
Наиболее близко к ядру расположен К-слой, затем идёт L-cлой, М-слой, N-cлой, ... В каждом слое оболочки с меньшими l характеризуются большей электронной плотностью вблизи ядра. Прочность связи электрона уменьшается с увеличением n, а при заданном n — с увеличением l; на рис. 5 схематически показаны (без соблюдения масштаба энергий) уровни энергии отдельного электрона в сложном Атом Чем слабее связан электрон в соответствующей оболочке, тем выше лежит его уровень энергии. Ядро с заданным Z присоединяет электроны в порядке уменьшения прочности их связи: сначала два электрона 1s, затем два электрона 2s, шесть электронов 2p и т. д. в соответствии со схемой рис. 5. Это определяет электронные конфигурации, т. е. распределения электронов по оболочкам, для ионов и нейтрального Атом данного элемента. Например, для азота (Z = 7) получаются электронные конфигурации
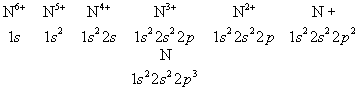
(число электронов в данной оболочке указывается индексом справа сверху). Такие же электронные конфигурации, как и ионы азота, имеют нейтральные атомы последовательных элементов в периодической системе, обладающие тем же числом электронов: Н, Не, Li, Be, В, С (Z = 1,2,3,4,5,6). Периодичность в свойствах элементов определяется сходством внешних электронных оболочек Атом Например, нейтральные Атом Р, As, Sb, Bi (Z = 15, 33, 51, 83) имеют по три р-электрона во внешней электронной оболочке подобно Атом N и схожи с ним по химическим и многим физическим свойствам.
При рассмотрении заполнения электронных оболочек необходимо учитывать, что, начиная с n = 4, электроны с меньшим l, но большим n, связываются прочнее, чем электроны с большим l, но меньшим n, например электроны 4s связаны прочнее, чем электроны 3d. Это отражает рис. 5, показывающий расположение уровней энергии, соответствующее действительному порядку (несколько схематизированному) заполнения электронных оболочек для последовательных элементов в периодической системе элементов Д. И. Менделеева. Числа, стоящие справа у скобок, определяют числа элементов в периодах этой системы, заканчивающихся атомами инертных газов с внешними оболочками типа nр6 (n = 2, 3, 4, 5, 6) для Ne, Ar, Kr, Xe, Rn (Z = 10, 18, 36, 54, 86).
Уровни энергии сложных атомов. Каждый Атом характеризуется нормальной электронной конфигурацией, получающейся, когда все электроны в Атом связываются наиболее прочно, и возбуждёнными электронными конфигурациями, когда один или несколько электронов связаны более слабо — находятся на более высоких уровнях энергии. Например, для Атом гелия наряду с нормальной электронной конфигурацией 1s2 возможны возбуждённые: 1s 2s, 1s 2p, ... (возбуждён один электрон), 2s"2, 2s2p, ... (возбуждены оба электрона). Определённой электронной конфигурации соответствует один уровень энергии Атом в целом, если электронные оболочки целиком заполнены (например, нормальная конфигурация Атом Ne 1s2 2s2 2p6), и ряд уровней энергии, если имеются частично заполненные оболочки (например, нормальная конфигурация A. N 1s2 2s2 2p3, для которой оболочка 2p заполнена как раз наполовину). При наличии частично заполненных d- и f-oболочек число уровней энергии, соответствующих каждой конфигурации, может достигать многих сотен, так что схема уровней энергии Атом с частично заполненными внешними оболочками получается очень сложной. Основным уровнем энергии Атом является самый нижний уровень нормальной электронной конфигурации.
Квантовые переходы в атоме. При квантовых переходах Атом переходит из одного стационарного состояния в другое — с одного уровня энергии на другой. При переходе с более высокого уровня энергии Ei на более низкий Ek Атом отдаёт энергию Ei—Ek, при обратном переходе получает её. Как для любой квантовой системы, для Атом квантовые переходы могут быть двух типов: с излучением (оптические переходы) и без излучения (безызлучательные или неоптические переходы). Важнейшая характеристика квантового перехода — вероятность перехода, определяющая, как часто этот переход будет происходить.
Квантовые переходы с излучением. При этих переходах Атом поглощает (переход Ek ® Ei) или испускает (переход EI ® Ek) электромагнитное излучение, например видимый свет, ультрафиолетовые лучи, инфракрасные лучи, СВЧ (микроволновое) излучение. Электромагнитная энергия поглощается и испускается Атом в виде кванта света — фотона, характеризуемого определённой частотой колебаний v, согласно соотношению:
Ei—Ek = hv, (8)
где h — постоянная Планка; hv — энергия фотона. Закон (8) представляет собой закон сохранения энергии для микроскопических процессов, связанных с излучением.
Атом в основном состоянии может только поглощать фотоны, а Атом в возбуждённых состояниях может как поглощать, так и испускать их. Свободный Атом в основном состоянии может существовать неограниченно долго; продолжительность пребывания Атом в возбуждённом состоянии — время жизни на возбуждённом уровне энергии — ограничена, Атом спонтанно, т. е. самопроизвольно, частично или полностью теряет энергию возбуждения, испуская фотон и переходя на более низкий уровень энергии (наряду с таким спонтанным испусканием возможно и вынужденное испускание, происходящее, подобно поглощению, под действием фотонов той же частоты; см. Квантовые переходы). Время жизни возбуждённого Атом тем меньше, чем больше вероятность спонтанного перехода. Для возбуждённых Атом водорода это время порядка 10—8 сек.
Совокупность частот возможных переходов с излучением определяет оптический спектр соответствующего Атом: совокупность частот переходов с нижних уровней на верхние — его спектр поглощения, совокупность частот переходов с верхних уровней на нижние — его спектр испускания. Каждому такому переходу соответствует определённая спектральная линия. Для Атом водорода, согласно формулам (4) и (8), получаем совокупность спектральных линий с частотами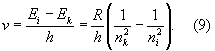
При nk = 1 и nI = 2, 3, 4, 5, ... получается спектральная серия Лаймана (линии La, Lb., Lg,...), при nk = 2 и ni= 3, 4,5,... — серия Бальмера (линии Нa, Hb, Нg ...), при nk = 3 и nI = 4, 5, ... — серия Пашена (рис. 1, б). Для Атом других элементов в соответствии с более сложной схемой уровней энергии получается и более сложный спектр (см. Атомные спектры).
Квантовые переходы без излучения. При этих переходах Атом получает или отдаёт энергию при взаимодействии с другими частицами, с которыми он сталкивается в газе или длительно связан в молекуле, жидкости или твёрдом теле. В газе Атом можно считать свободным в промежутках времени между столкновениями; во время столкновения (удара) Атом может, благодаря кратковременному взаимодействию, перейти на другой уровень энергии. Такое столкновение называется неупругим (в противоположность упругому столкновению, при котором изменяется только кинетическая энергия поступательного движения Атом, а его внутренняя энергия остаётся неизменной). Важный частный случай — столкновение свободного Атом с электроном; обычно электрон движется быстро по сравнению с Атом, время столкновения очень мало и можно говорить об электронном ударе. Возбуждение Атом электронным ударом является одним из методов определения уровней энергии Атом Вероятности неупругих столкновений и, в частности, возбуждения А" электронным ударом могут быть рассчитаны методами квантовой механики (см. Столкновения атомные).
Химические и физические свойства атома. Большинство свойств Атом определяется строением и характеристиками его внешних электронных оболочек, в которых электроны связаны сравнительно слабо (энергии связи от нескольких эв до нескольких десятков эв). Строение внутренних оболочек Атом, электроны которых связаны гораздо прочнее (энергии связи в сотни, тысячи и десятки тысяч эв), проявляется лишь при взаимодействиях Атом с быстрыми частицами и фотонами больших энергий (более сотен эв.) Такие взаимодействия определяют рентгеновские спектры Атом и рассеяние атомом быстрых частиц (см. Рассеяние микрочастиц, Дифракция частиц). От массы Атом, определяемой массой его ядра, зависят его механические свойства при движении Атом как целого — количество движения, кинетическая энергия. От механических и связанных с ними магнитных и электрических моментов Атом зависят некоторые тонкие эффекты, проявляющиеся при изучении физических свойств Атом (см. Моменты атомных ядер, Ядерный магнитный резонанс, Ядерный квадрупольный резонанс, Сверхтонкая структура).
Свойства атома, определяемые его внешними электронами. Электроны во внешних оболочках Атом, связанные сравнительно слабо, легко подвергаются внешним воздействиям. При сближении данного Атом с другими возникают сильные электростатические взаимодействия (включая т. н. обменные взаимодействия), которые могут приводить к возникновению химической связи Атом, т. е. к образованию молекулы. В химической связи участвуют электроны внешних оболочек; в случае ковалентной связи эти электроны принадлежат уже не отдельным Атом, а образовавшейся молекуле в целом, и входят в состав её молекулярных электронных оболочек. Т. о., внешние электроны Атом определяют его химические свойства.
Более слабые электростатические взаимодействия двух Атом проявляются в их взаимной поляризации — смещении электронов относительно ядер, наиболее сильном для слабо связанных внешних электронов (см. Поляризация частиц). Возникают поляризационные силы притяжения между Атом, которые надо учитывать уже на больших расстояниях между ними (см. Межмолекулярное взаимодействие). Поляризация Атом происходит и во внешних электрических полях; в результате уровни энергии Атом смещаются и, что особенно важно, вырожденные уровни энергии расщепляются (поляризация различна для различных квантовых состояний Атом, соответствующих той же его энергии) — имеет место Штарка явление. Поляризация Атом может возникнуть под действием электрического поля световой (электромагнитной) волны; она зависит от частоты света, что обусловливает зависимость от неё и показателя преломления (см. Дисперсия света), связанного со способностью Атом поляризоваться — с поляризуемостью Атом (см. Поляризуемость атомов, ионов и молекул). Тесная связь оптических характеристик Атом с его электрическими свойствами особенно ярко проявляется в его оптических спектрах.
Внешними электронами определяются и магнитные свойства Атом Они схожи для элементов с аналогичными внешними электронными оболочками Атом Магнитный момент Атом зависит от его механического момента (см. Магнитомеханическое отношение), в Атом с полностью заполненными электронными оболочками он равен нулю, так же как и механический момент. При наличии частично заполненных внешних электронных оболочек магнитные моменты Атом, как правило, постоянны, и Атом являются парамагнитными (см. Парамагнетизм). Во внешнем магнитном поле все уровни Атом, у которых магнитный момент не равен нулю, расщепляются (см. Зеемана явление). Все Атом обладают диамагнетизмом, который обусловлен возникновением у них магнитного момента под действием магнитного поля (т. н. индуцированного магнитного момента, аналогичного электрическому дипольному моменту Атом).
Свойства ионизованного атома. При последовательной ионизации Атом, т. е. при отрыве его электронов, начиная с самых внешних, в порядке увеличения прочности их связи (рис. 5), соответственно изменяются все свойства Атом, определяемые его внешней оболочкой. Внешними становятся все более прочно связанные электроны; в результате сильно уменьшается способность Атом поляризоваться в электрическое поле, увеличиваются расстояния между уровнями энергии и частоты оптических переходов между этими уровнями (что приводит к смещению спектров в сторону всё более коротких длин волн). Ряд свойств обнаруживает периодичность: сходными оказываются свойства ионов с аналогичными внешними электронами, например N7+ и N3+ (один и два электрона 2s) обнаруживают сходство с N6+ и N5+ (один и два электрона 1s). Это относится к характеристикам и относительному расположению уровней энергии и к оптическим спектрам, к магнитным моментам Атом и т. д. Наиболее резкое изменение свойств происходит при удалении последнего электрона из внешней оболочки, когда остаются лишь полностью заполненные оболочки; например при переходе от N4+ к N5+ (электронные конфигурации 1s22s и 1s2). В этом случае ион наиболее устойчив и его полный механический и полный магнитный моменты равны нулю. Особенно устойчивы, помимо ионов с электронной конфигурацией 1s2, ионы с полностью заполненной внешней оболочкой nр(n = 2, 3, 4, ...).
Свойства связанных атомов. Свойства Атом, находящегося в связанном состоянии, например входящего в состав молекулы, отличаются от свойств свободного Атом Наибольшие изменения претерпевают свойства Атом, определяемые самыми внешними электронами, принимающими участие в присоединении данного Атом к другому. Вместе с тем свойства, определяемые электронами внутренних оболочек, могут практически не измениться, как это имеет место для рентгеновских спектров. Некоторые свойства Атом могут испытывать сравнительно небольшие изменения, по которым можно получить информацию о характере взаимодействий связанных Атом Важным примером может служить расщепление уровней энергии Атом в кристаллах и комплексных соединениях, которое происходит под действием электрических полей, создаваемых окружающими ионами (см. Кристаллического поля теория).
Лит. см. при ст. Атомная физика.
М. Атом Ельяшевич.
| "БСЭ" >> "А" >> "АТ" >> "АТО" |
Статья про "Атом" в Большой Советской Энциклопедии была прочитана 1924 раз
| Бургер двойного помола |
| Семга на горелке |
TOP 20
- Лемке Михаил Константинович
- Сульфгидрильные группы
- «Казарменный коммунизм»
- Японское море
- Периодическая система элементов
- Башкирская Автономная Советская Социалистическая Республика
- Объединённая партия гаитянских коммунистов
- Глициния
- Иммунитет (историч.)
- Андаманское море
- Сенсуализм
- Балкано-кавказская раса
- «Сообразительный»
- Навигация (морск.)
- Звёздная астрономия
- Ямполь (пос. гор. типа в Донецкой обл.)
- Мандельштама - Бриллюэна рассеяние
- Театральные учебные заведения
- Кульчицкая Елена Львовна
- Электрическая постоянная